En juin 2023, les associations de la Fédération SOS GLOBI participeront à la Course des Héros. Ce défi sportif solidaire, nous permet de sensibiliser le grand public à la drépanocytose et à la thalassémie!
QU'EST-CE QUE LA COURSE DES HÉROS?
La course des héros est un défi sportif solidaire organisé au mois de juin.
Cet évènement permet aux associations de renforcer leur visibilité et de sensibiliser à une cause au travers d’un grand évènement national.
Chaque participant s’inscrit pour une association et s’engage à récolter des dons qui seront reversés à l’association choisie.
Depuis 2017 notre organisation a choisit de participer à la course des héros en présentiel, dans les villes où nos associations de proximité sont actives et de manière virtuelle pour permettre au plus grand nombre de participer. Les participants en présentiel relèvent le défi de la course à pied ou de la marche. En virtuel, les participants peuvent partout en France relever le défi sportif de leur choix (marche, course à pieds, vélo…) seuls ou en groupe lors d’une activité organisée par l’association SOS Globi de proximité.
Grâce à l’extraordinaire mobilisation des patients, des soignants et des bénévoles , notre organisation réussi à collecter des dizaines de milliers d’euros chaque année afin de
- Soutenir les activités annuelles des associations de proximité (les cagnottes ont été reversées aux associations de proximité qui le souhaitaient).
- Maintenir nos activités d’information, de sensibilisation et de défense des patients à l’échelle nationale via la Fédération SOS Globi
- Financer le projet de création d’une fondation de recherche pour la drépanocytose
LE DÉFI SOS GLOBI
Organisée autour du mois de juin, la Course des Héros est une formidable opportunité pour nos associations de communiquer autour de la drépanocytose et de la thalassémie.
En effet les mois de mai et juin sont dédiés à la sensibilisation, en lien avec les journées mondiales de la thalassémie (8 mai) et de la drépanocytose (19 juin).
Depuis 2017, les bénévoles de nos associations participent à la Course des Héros afin de:
- Sensibiliser le grand public à nos pathologies
- Collecter des fonds au profit de nos actions
- Fédérer les acteurs impliqués dans ces pathologies (patients, familles, professionnels de santé, sociétés pharmaceutiques…) autour d’un évènement solidaire
EN 2023, REJOIGNEZ NOS HÈROS!
Vous avez envie de relever un défi sportif et vous êtes intéressés pour soutenir nos associations?
Vous pouvez nous contacter à l’adresse contact@sosglobi.fr
Vous êtes un entreprise et votre équipe souhaite s’engager pour notre association?
Contactez- nous!
Informations et liens utiles:
Consulter le site de la Course des Héros!
Inscrivez-vous pour participer à la Course des Héros 2023
Téléchargez notre dossier Course des Héros -Défi SOS GLOBI 2023
Soutenez nos Héros, faites un don!









 crédit photo https://sportadapte.fr/pratiquer/formes-de-pratique/sport-sante/
crédit photo https://sportadapte.fr/pratiquer/formes-de-pratique/sport-sante/





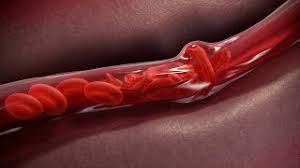




 Photo du site https://www.the-scientist.com/news-opinion/a-new-way-to-establish-cause-and-effect-in-epidemiology--66871
Photo du site https://www.the-scientist.com/news-opinion/a-new-way-to-establish-cause-and-effect-in-epidemiology--66871
 Photo provenant du site
https://france3-regions.francetvinfo.fr/occitanie/haute-garonne/toulouse/covid-hospitalisation-domicile-soulager-services-hospitaliers-toulouse-1889562.html
Photo provenant du site
https://france3-regions.francetvinfo.fr/occitanie/haute-garonne/toulouse/covid-hospitalisation-domicile-soulager-services-hospitaliers-toulouse-1889562.html
 Photo provenant du site
https://www.medgrouppa.com/news/181-empowering-patients-to-self-manage
Photo provenant du site
https://www.medgrouppa.com/news/181-empowering-patients-to-self-manage